炒股就看金麒麟分析师研报,权威,专业,及时,全面,助您挖掘潜力主题机会!
2 月 10 日,石药集团宣布,其附属公司石药集团巨石生物开发的注射用奥马珠单抗生物类似药(商品名:恩益坦)的新适应症已获得 NMPA 批准上市,用于治疗中至重度持续性过敏性哮喘。这是该药在中国获批的第 2 个适应症。
公告
恩益坦是石药集团开发的一款人免疫球蛋白 E(IgE)人源化单克隆抗体,为茁乐(罗氏和诺华开发)的生物类似药。此前,恩益坦已于 2024 年 9 月获批上市,用于治疗采用 H1 抗组胺药治疗后仍有症状的成人和青少年(12 岁及以上)慢性自发性荨麻疹患者,是国内首个以生物制品 3.3 类注册分类获批上市的奥马珠单抗生物类似药。
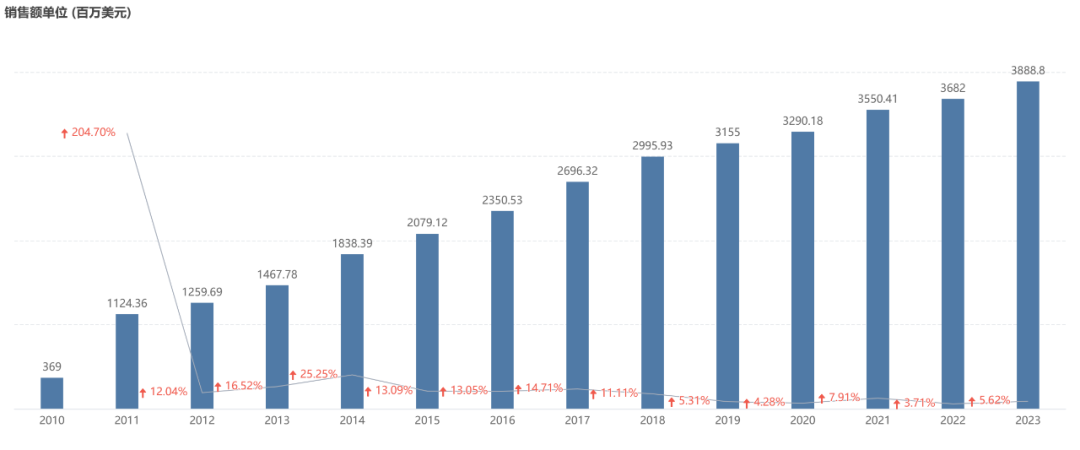
奥马珠单抗原研药茁乐(海外商品名 Xolair)由罗氏(负责美国市场)和诺华(负责其它市场)联合开发,是自免领域的重磅炸弹级别药物。自上市以来,该药的销售额也是一路上涨。2023 年度,在上市 21 年后,它的全球销售额依然实现了 5.6% 的增长至 38.89 亿美元。
根据诺华和罗氏的 2024 年财报,茁乐去年的全球销售额为 44.49 亿美元,同比增长 14%。不过,罗氏在财报中指出,Xolair 的基本、主要专利已到期,其配方专利将于 2025 年底在美国到期,预计该药的首批生物类似药将于 2026 年在美国上市。
在国内,除了原研外,目前已经由两款国产奥马珠单抗获批:一款来自迈博药业(CMAB007,注册分类为 3.4),获批治疗过敏性哮喘;另一款来自石药集团(SYN008,注册分类 3.3),获批治疗慢性自发性荨麻疹、过敏性哮喘。
文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担, 关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部责任。本公众号发布的各类文章重在分享,如有侵权请联系我们,我们将会删除。
(转自:求实药社)






还没有评论,来说两句吧...